科学家揭示新冠病毒引发致命'第二阶段“机制
科学家揭示新冠病毒引发致命“第二阶段”的关键在于对血管内皮细胞的直接和间接损伤,尤其是肺部血管内皮细胞。
说实在话,医界专家和医生们对新冠病毒致病和致命原因仍然只知皮毛。
作者:全球医生组织
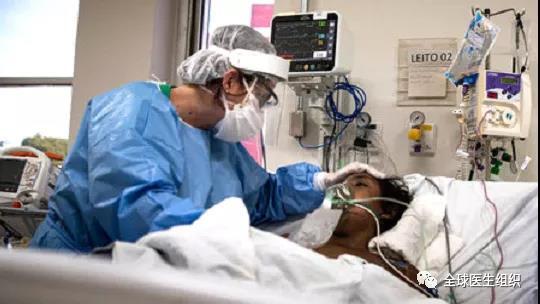
3月初,苏黎世大学医院心脏病科主任鲁斯奇兹卡注意到新冠病毒感染患者出现了奇怪症状,人们认为主要是呼吸道病毒感染所致。鲁斯奇兹卡邀请病理学家在第一位患者死亡之前做好尸检准备。
许多新冠病毒感染患者出现了急性肾衰竭、器官损害和不明原因血栓。几周后,第一例尸体解剖发现:肺部毛细血管布满了微小血栓和坏死细胞、炎症反应使供应身体器官的各种血管出现了不同程度的扩张。病理学家说从未见过此种病理改变。
尸检报告也让鲁斯奇兹卡意识到患者遭受巨大痛苦的原因"病毒以患者的血管系统为攻击目标”。
自从苏黎世研究小组的临床发现在4月中旬发表以来,数十项临床研究报告接二连三地报告了死于冠病毒感染患者类似的血管损伤模式。
5月21日,国际权威期刊《新英格兰医学杂志》发表了一篇论文揭示冠病毒感染患者的肺部组织血栓数量是死于H1N1流感患者的9倍。
还有一些其他临床研究也报告了儿童感染的炎症症状;健康年轻人的突发中风等等。
目前,研究人员正在把这些临床研究发现形成一种新的疾病假设,来解释一些患者在住院1周左右后就进入了病毒感染致命的“第二阶段”的原因。
比利时VIB研究所的血管生物学家彼得•卡米利特指出,新冠病毒引发致命“第二阶段”的关键在于对血管内皮细胞的直接和间接损伤,尤其是肺部血管内皮细胞。
通过攻击这些内皮细胞,新冠病毒感染导致血管大量渗出和血液凝固。这些变化引发全身炎性反应,进而引发急性呼吸窘迫综合征(ARDS),最终导致患者死亡。
这种机制可以解释一些肥胖症、糖尿病和心血管疾病等基础疾病的患者,易于发展成为重症的原因:“这些患者的血管内皮细胞已经受到损伤了”。
如果这种假设成立,用于治疗血管疾病的药物将有助于防止新冠病毒感染患者发展为危重症。
美国辛辛那提大学医学院心脏病学家理查德博士近日在《血栓和溶栓杂志》上发表了一篇综述,概述了类似的心血管级联。他认为在安全有效疫苗出现之前,这种针对血管疾病的疗法将会成为“一个良好开端”。
正常人体中血管内皮细胞能够协助调节血压,抑制炎症和凝血,部分功能是通过持续产生一氧化氮(NO)来实现的。当血管受损时,它们会向免疫细胞和凝血因子发出一系列复杂信号,这些细胞会迅速修复受损部位。同时也会警告其他内皮细胞警惕“入侵者”。
根据苏黎世医院专家的尸检报告,流行病学研究以及新冠病毒在实验室细胞中的作用机制,专家们认为病毒会使得该血管内皮细胞调节系统失控。
当新冠病毒进入肺部时,它会侵入肺泡中的细胞,这些肺泡周围布满了毛细血管,血管内皮细胞整齐排列。
新冠病毒进入肺部时,攻击排列在肺泡周围血管的内皮细胞。受伤的内皮细胞会导致液体从微血管中渗出,引发血凝并激发大量免疫细胞和信使因子导致更广泛的炎性反应。
当病毒直接侵入其中一些细胞时,其他的内皮细胞则被“激活”,会对来自入侵病毒和其他受损细胞的信号做出反应。一些受感染的细胞可能会自杀,释放出一些信号。
研究人员认为,被激活细胞的损伤和其他变化引发血管渗漏,使肺泡充满液体,这是急性呼吸窘迫综合征的特征之一。
白细胞大量涌向肺部,与激活的内皮细胞一起,免疫细胞释放大量信号分子,包括白细胞介素,促使局部血压升高,削弱细胞连接。内皮细胞损伤也暴露了血管内膜层。
暴露的内膜反过来引发不受控制的凝血机制。内皮细胞和免疫细胞吸附了大量的凝血因子和血小板,加速了凝血过程。
这些血块降解成关键的生物标志物D-二聚体,其水平急剧增高提醒临床医生病情紧急。最终,这种凝血会扩散到全身,阻断重要器官的血液供应,危及患者生命。
无论怎样,医生取得的每一点点知识和临床经验都是无辜患者付出的代价,甚至是生命。急需共享临床宝贵经验和教训,挽救更多的患者生命。









